Intelligenza artificiale e photon-counting CT
Le tre fasi della rivoluzione software–hardware in radiologia
L’evoluzione recente dell’imaging radiologico è guidata da due innovazioni convergenti: l’intelligenza artificiale (IA) e la photon-counting computed tomography (PCCT). Se l’IA rappresenta una rivoluzione cognitiva nella capacità di analizzare e interpretare i dati, la PCCT introduce una trasformazione fisica nella formazione dell’immagine, grazie a rivelatori capaci di contare singoli fotoni e discriminare la loro energia. L’integrazione tra queste tecnologie sta ridefinendo il paradigma della diagnostica radiologica.
Uno schema concettuale proposto recentemente descrive questa evoluzione attraverso tre fasi progressive: assistenza, partnership e autonomia, che riflettono il modo in cui software e hardware stanno trasformando la pratica clinica.
Fase 1 – Assistenza: dall’immagine alla quantificazione
Nella prima fase, l’IA agisce come strumento di supporto al radiologo, automatizzando compiti ripetitivi e migliorando l’efficienza del workflow.
Tra le principali applicazioni:
- Rilevazione automatica di noduli, emorragie intracraniche o altre lesioni.
- Segmentazione degli organi e quantificazione di parametri come il grasso epatico o il volume tumorale.
- Riduzione dei tempi di analisi, grazie alla sostituzione di procedure manuali con algoritmi automatici.
Parallelamente, la photon-counting CT introduce un nuovo livello di qualità dell’immagine: maggiore risoluzione spaziale, riduzione del rumore elettronico e possibilità di ottenere mappe quantitative dei materiali. Tuttavia, né l’IA né la tecnologia di rivelazione possiedono capacità interpretative autonome: il radiologo rimane il decisore finale nel distinguere tra lesioni reali, artefatti o varianti anatomiche.
Fase 2 – Partnership: l’alleanza cognitivo-spettrale
La seconda fase rappresenta un passaggio da semplice assistenza a collaborazione tra radiologo e algoritmo.
I nuovi modelli di IA multimodale sono in grado di integrare:
- dati di imaging,
- informazioni cliniche,
- risultati di laboratorio,
- dati genomici.
In questo contesto, la PCCT fornisce informazioni spettrali intrinseche, come:
- immagini monoenergetiche virtuali,
- decomposizione dei materiali,
- mappe quantitative di iodio o calcio.
L’IA può analizzare queste informazioni per caratterizzare i tessuti oltre le capacità percettive umane, ad esempio distinguendo tra tessuto tumorale vitale e necrosi o identificando caratteristiche di placca aterosclerotica. Questa fase introduce anche il concetto di explainable AI, in cui gli algoritmi mostrano quali caratteristiche dell’immagine influenzano la decisione diagnostica.
Fase 3 – Autonomia e supervisione
La terza fase prevede sistemi con autonomia operativa parziale, già osservabili in alcuni workflow clinici.
Nei contesti di emergenza, ad esempio:
- l’IA può analizzare automaticamente le TC prima della revisione umana;
- gli esami sospetti vengono prioritizzati nella lista di lavoro;
- vengono generati alert preliminari per patologie critiche come ictus o trauma.
Con la PCCT, l’enorme volume di dati spettrali rende sempre più importante l’automazione per la gestione e l’analisi delle informazioni. Tuttavia, è fondamentale distinguere tra autonomia di workflow e autonomia diagnostica: i sistemi di IA possono supportare la gestione e la triage degli esami, ma la responsabilità diagnostica rimane necessariamente del radiologo.
Messaggio chiave
La combinazione tra intelligenza artificiale e photon-counting CT rappresenta la convergenza tra intelligenza cognitiva e innovazione fisica dell’imaging. Questa evoluzione non sostituisce il radiologo, ma ne trasforma il ruolo: da interprete dell’immagine a supervisore di ecosistemi diagnostici sempre più complessi e quantitativi.
Per approfondire
Scaglione M., Brunetti A., Fanni S. C., Neri E., Masala S. A.
Artificial intelligence and photon-counting CT: the three phases of the software–hardware revolution in radiology.
La Radiologia Medica (2026).
https://doi.org/10.1007/s11547-026-02193-1
Masse renali e malattia renale cronica: una sfida diagnostica
Il ruolo dell’ecografia con mezzo di contrasto (CEUS) oltre i limiti di TC e RM
La gestione del carcinoma renale (RCC) nei pazienti con malattia renale cronica (CKD) è estremamente complessa. Se da un lato la CKD aumenta il rischio di sviluppare tumori maligni, dall’altro le alterazioni strutturali del rene e le restrizioni all’uso di mezzi di contrasto iodati o a base di gadolinio rendono le metodiche radiologiche convenzionali spesso inconclusive. In questo scenario, la CEUS emerge come una soluzione sicura ed efficace.
Il contesto: i limiti dell’imaging tradizionale
Nei pazienti con insufficienza renale avanzata, la diagnosi è ostacolata da diversi fattori tecnici e clinici:
- Riduzione della cospicuità: la distorsione architettonica e l’ipoperfusione tipiche della CKD riducono il contrasto naturale tra lesione e parenchima.
- Masse indeterminate: l’impossibilità di utilizzare contrasti nefrotossici in fase avanzata o dialitica lascia molte masse senza una caratterizzazione certa dopo TC o RM basale.
- Pseudotumori: materiale proteicaceo o emorragico all’interno di cisti (comuni nella malattia cistica acquisita o ACKD) può simulare un enhancement solido, portando a falsi positivi.
La soluzione: i vantaggi della CEUS
L’ecografia con mezzo di contrasto affronta direttamente queste criticità grazie alle proprietà uniche dei microbolle:
- Sicurezza renale: i mezzi di contrasto per ecografia sono puramente intravascolari e non vengono escreti dai reni, rendendoli sicuri in tutti gli stadi della CKD e nei pazienti in dialisi.
- Risoluzione temporale: la visualizzazione in tempo reale del microcircolo permette di distinguere setti vascolarizzati, ispessimenti parietali e noduli murali da detriti avascolari.
- Caratterizzazione delle lesioni: la CEUS eccelle nella classificazione delle lesioni cistiche (Bosniak) e nella differenziazione tra masse solide benigne e maligne, guidando la scelta tra chirurgia e sorveglianza attiva.
Messaggio chiave
La CEUS rappresenta lo strumento d’elezione per colmare il gap diagnostico nelle masse renali associate a CKD. Grazie alla sua eccellente sicurezza e alla capacità di fornire una valutazione microvascolare dettagliata, permette di evitare biopsie invasive o interventi non necessari, ottimizzando il percorso di cura in una popolazione di pazienti particolarmente fragile.
Per approfondire
Eusebi L., Masino F., Montatore M., et al. Diagnostic evaluation of renal masses in chronic kidney disease: a clinical and radiologic challenge. Abdominal Radiology (2026). https://doi.org/10.1007/s00261-026-05491-4
Sarcopenia e risposta alla chemioterapia nel carcinoma vescicale
Il ruolo dell’intelligenza artificiale nella valutazione della composizione corporea
Nel carcinoma vescicale muscolo-invasivo (MIBC), la chemioterapia neoadiuvante (NAC) rappresenta lo standard terapeutico prima della cistectomia radicale. Tuttavia, la risposta al trattamento è altamente variabile e non tutti i pazienti traggono beneficio da questo approccio. Un recente studio ha valutato il ruolo della sarcopenia, misurata mediante analisi automatizzata con intelligenza artificiale su TC, come possibile biomarcatore predittivo di risposta alla NAC.
I risultati suggeriscono che l’analisi della composizione corporea potrebbe contribuire alla stratificazione prognostica dei pazienti e alla personalizzazione delle strategie terapeutiche.
Il contesto: quando la composizione corporea diventa un biomarcatore
La sarcopenia è caratterizzata da una riduzione della massa muscolare scheletrica ed è sempre più riconosciuta come fattore prognostico negativo in diversi tumori solidi. Nei pazienti oncologici è stata associata a maggiore tossicità terapeutica, peggior outcome e minore risposta ai trattamenti sistemici.
Grazie ai recenti sviluppi dell’intelligenza artificiale, la quantificazione della massa muscolare può essere effettuata automaticamente su TC già eseguite per lo staging oncologico, trasformando un esame routinario in una fonte di informazioni prognostiche aggiuntive.
Lo studio: analisi automatizzata della massa muscolare
Lo studio ha analizzato pazienti con carcinoma vescicale non metastatico sottoposti a chemioterapia neoadiuvante seguita da cistectomia radicale.
Metodologia:
- Valutazione della sarcopenia: un software basato su intelligenza artificiale ha calcolato automaticamente lo Skeletal Muscle Index (SMI) dalle immagini TC al livello della vertebra L3.
- Valutazione della risposta: la risposta alla terapia è stata analizzata mediante NacVI-RADS, sistema di reporting basato su risonanza magnetica multiparametrica.
- Analisi statistica: è stata valutata la relazione tra sarcopenia e risposta patologica alla NAC.
I risultati: un predittore indipendente di non risposta
L’analisi ha evidenziato una significativa associazione tra sarcopenia e mancata risposta alla chemioterapia neoadiuvante.
Principali risultati:
- Prevalenza: circa un terzo dei pazienti presentava sarcopenia al momento della diagnosi.
- Associazione clinica: i pazienti sarcopenici mostravano una probabilità significativamente maggiore di non risposta alla NAC.
- Analisi multivariata: la sarcopenia è risultata un predittore indipendente di scarsa risposta al trattamento.
- Performance diagnostica: lo SMI ha dimostrato un’elevata capacità discriminativa nell’identificare i pazienti non responder.
Implicazioni cliniche: verso una stratificazione personalizzata
L’integrazione dell’analisi automatizzata della composizione corporea nei workflow radiologici potrebbe migliorare la selezione dei pazienti candidati alla chemioterapia neoadiuvante.
In particolare, l’identificazione precoce della sarcopenia potrebbe:
- supportare strategie di ottimizzazione nutrizionale e metabolica prima del trattamento;
- contribuire alla selezione dei pazienti più idonei alla NAC;
- favorire un approccio più personalizzato alla terapia oncologica.
Poiché l’analisi si basa su immagini TC già disponibili nella pratica clinica, questa valutazione può essere integrata nel referto radiologico senza necessità di esami aggiuntivi.
Messaggio chiave
La valutazione della sarcopenia mediante intelligenza artificiale su TC emerge come biomarcatore imaging promettente per predire la risposta alla chemioterapia neoadiuvante nel carcinoma vescicale muscolo-invasivo. L’integrazione di queste analisi quantitative potrebbe migliorare la stratificazione prognostica e contribuire allo sviluppo di strategie terapeutiche sempre più personalizzate.
Per approfondire
Borrelli A., Novelli S., Messina E., et al.
AI-assessed sarcopenia as an independent predictor of neoadjuvant chemotherapy outcomes in muscle-invasive bladder cancer.
La Radiologia Medica (2026).
https://doi.org/10.1007/s11547-026-02203-2
IA e screening opportunistico: predire il rischio di fratture vertebrali
Radiomica e TC per la gestione del tumore al seno in terapia ormonale
Le donne sottoposte a terapie di deprivazione estrogenica (HDT) per il tumore al seno presentano un rischio significativamente elevato di fragilità ossea. Tuttavia, la sola densitometria ossea (MOC-DEXA) spesso non è sufficiente a predire accuratamente il rischio di fratture. Un recente studio esplora come l’intelligenza artificiale applicata alle comuni scansioni TC (screening opportunistico) possa colmare questo gap diagnostico.
Il contesto: oltre la densità minerale ossea
Nelle pazienti in terapia ormonale, la microarchitettura ossea può deteriorarsi prima che si verifichi una riduzione significativa della densità minerale. La TC “opportunistica” , ovvero l’analisi di scansioni effettuate per altri motivi, come il follow-up oncologico, offre un’occasione unica per valutare la qualità dell’osso senza esami aggiuntivi.
Lo studio: radiomica e reti neurali
La ricerca ha utilizzato un approccio basato sull’IA per analizzare le vertebre lombari di 109 pazienti:
- Segmentazione automatica: una rete neurale convoluzionale (CNN) è stata impiegata per identificare e isolare automaticamente le vertebre nelle immagini TC.
- Analisi radiomica: sono state estratte centinaia di caratteristiche quantitative (RF) relative alla texture e alla forma dell’osso, invisibili all’occhio umano.
- Modello predittivo: è stato sviluppato un modello capace di distinguere tra pazienti che svilupperanno fratture vertebrali (VF) e quelle che rimarranno stabili.
I risultati: una nuova frontiera per la prevenzione
Il modello basato sulla radiomica ha mostrato prestazioni promettenti:
- Accuratezza: le caratteristiche di texture dell’osso si sono dimostrate predittori più affidabili rispetto ai parametri clinici tradizionali.
- Integrazione clinica: l’uso dell’IA permette di trasformare una TC di routine in uno strumento di screening preventivo per l’osteoporosi indotta da farmaci.
- Personalizzazione: identificare precocemente le pazienti ad alto rischio consente l’avvio tempestivo di terapie protettive (come i bisfosfonati), riducendo la morbilità a lungo termine.
Messaggio chiave
L’intelligenza artificiale applicata alla TC opportunistica rappresenta una svolta nella medicina di precisione per le pazienti oncologiche. Sfruttando dati già esistenti, il radiologo può fornire una valutazione del rischio di frattura accurata e personalizzata, migliorando significativamente la qualità di vita post-trattamento.
Per approfondire
Birtolo M. F., Levi R., Pagano M., et al. Artificial intelligence on opportunistic computed tomography for predicting vertebral fracture risk in women undergoing estrogen deprivation therapy for breast cancer. La Radiologia Medica (2026).
https://doi.org/10.1007/s11547-026-02172-6
Glossario radiologico
Caso clinico 1
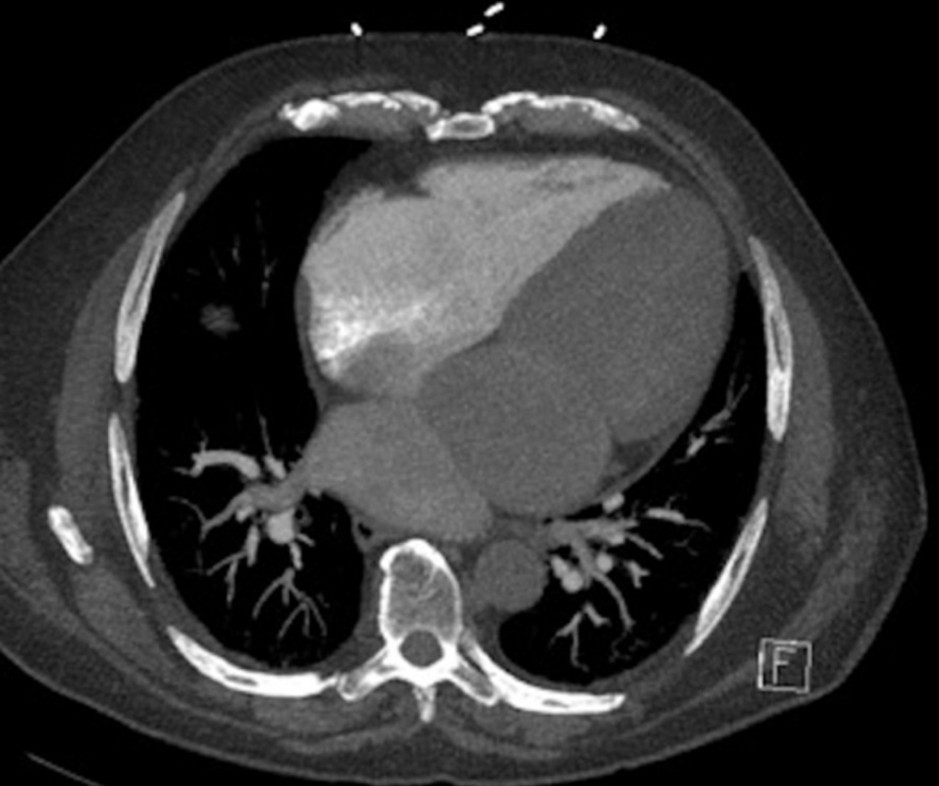
Donna di 41 anni con dispnea ingravescente, episodi sincopali e recente fibrillazione atriale. Ecocardiogramma dubbio per stenosi mitralica.
Quale meccanismo spiega la dilatazione delle vene polmonari in questo caso?
- Insufficienza mitralica funzionale
- Aumento della pressione nel compartimento prossimale dell’atrio sinistro
- Ridotta contrattilità ventricolare sinistra
- Shunt destro-sinistro
- Aumento della compliance venosa
Risposta corretta: B
COMMENTO
Nel car triatriatum, la camera prossimale riceve le vene polmonari ma è separata dalla valvola mitrale.
Se la fenestrazione è piccola:
- si crea un ostacolo al deflusso
- ↑ pressione nella camera prossimale
- trasmissione retrograda → ipertensione venosa polmonare
Questo spiega:
- dilatazione delle vene polmonari
- sintomi simili a stenosi mitralica
Caso clinico 2
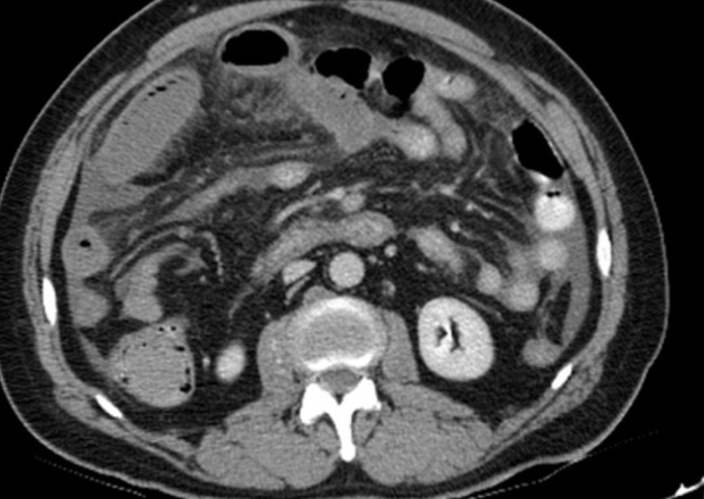
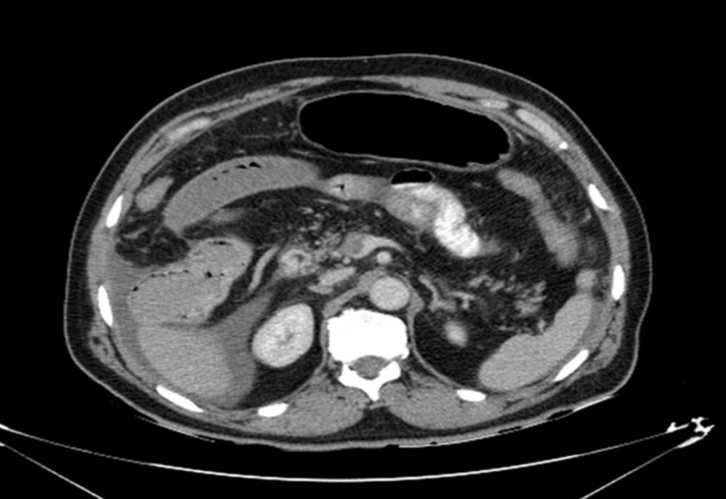
Paziente con dolore addominale severo, lattati elevati. APR: Fattore V di Leiden.
Perché la parete intestinale appare ipodensa nonostante sia presente enhancement mucoso?
- Vasospasmo arterioso diffuso
- Necrosi mucosa selettiva
- Edema sottomucoso da congestione venosa
- Riduzione del flusso arterioso
- Presenza di aria intramurale
Risposta corretta: C
COMMENTO
Nell’infarto venoso:
- il problema è nel deflusso → ↑ pressione capillare
- stravaso di liquidi → edema sottomucoso
- mucosa può ancora captare inizialmente
Risultato:
- pattern “a bersaglio”
- centro ipodenso (edema)
- mucosa periferica con enhancement
Insight: arterioso ≠ venoso
- arterioso → parete sottile, ipoenhancement
- venoso → parete ispessita, edema marcato
Caso clinico 3
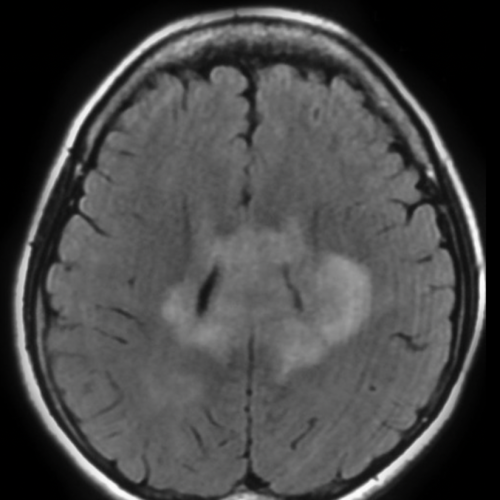
Uomo di 55 anni con cefalea e deficit cognitivo lieve. RM encefalo mostra una lesione periventricolare iperintensa in FLAIR e bilaterale. Viene iniziata terapia steroidea empirica → dopo 10 giorni la lesione si riduce drasticamente.
Qual è il meccanismo che spiega la drastica riduzione della lesione dopo terapia steroidea?
- Riduzione dell’edema vasogenico per stabilizzazione della barriera emato-encefalica
- Citotossicità diretta sugli oligodendrociti
- Apoptosi delle cellule tumorali linfomatose steroido-sensibili
- Riduzione della pressione intracranica
- Vasocostrizione arteriosa
Risposta corretta: C
COMMENTO
Questo è un classico (e pericoloso) scenario di linfoma primitivo del SNC.
Gli steroidi:
- inducono apoptosi dei linfociti neoplastici
- possono far “sparire” la lesione alla RM
Insight radiologico-clinico:
- lesione periventricolare + enhancement omogeneo + restrizione diffusiva
- forte sospetto di linfoma
Trappola:
- dare steroidi prima della biopsia può rendere la diagnosi impossibile
Questo è uno dei pochi tumori che regredisce rapidamente senza essere realmente curato.
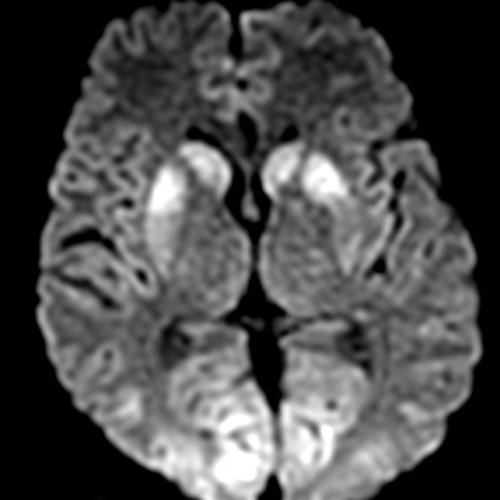
Caso clinico 4
Uomo di 47 anni trovato incosciente in casa. All’arrivo in PS: GCS 6, lattati elevati.
TC encefalo di base: negativa.
Perché il globo pallido bilateralmente è particolarmente vulnerabile nel danno da ipossia/monossido di carbonio?
- Maggiore permeabilità della barriera emato-encefalica
- Elevata densità di recettori glutammatergici
- Maggior contenuto di mielina
- Ridotta vascolarizzazione arteriosa
- Alto metabolismo ossidativo e vulnerabilità allo stress mitocondriale
Risposta corretta: E
COMMENTO
Il globo pallido rappresenta una delle strutture più sensibili all’ipossia e alla tossicità da monossido di carbonio per ragioni strettamente metaboliche.
Questa regione è caratterizzata da:
- elevata richiesta energetica
- intensa attività ossidativa mitocondriale
- dipendenza critica dalla fosforilazione ossidativa
Il monossido di carbonio esercita il suo effetto tossico attraverso:
- legame con la citocromo c ossidasi
- inibizione della catena di trasporto degli elettroni
- compromissione della produzione di ATP
Ne consegue un rapido fallimento energetico cellulare con sviluppo di edema citotossico, che si manifesta come restrizione della diffusione nelle sequenze DWI.
Dal punto di vista radiologico, il coinvolgimento simmetrico dei globi pallidi è altamente suggestivo di eziologia metabolico-tossica. La predominanza pallidale rispetto ad altre strutture dei nuclei della base è un elemento distintivo classico dell’intossicazione da monossido di carbonio.
Il pattern di distribuzione del danno è fondamentale per l’inquadramento eziologico:
- distribuzione simmetrica → suggerisce causa sistemica/metabolica
- selettività anatomica → riflette vulnerabilità bioenergetica regionale
- coinvolgimento prevalente del pallido → orienta verso tossicità da CO (rispetto ad altre encefalopatie ipossiche o tossiche)